Titolazione dell’ acido fosforico nella " Coca cola "
Principi :
L’esperienza consiste nel titolare la nota bibita "coca cola" con una base, in modo tale da poter determinare l’effettiva concentrazione di H3PO4 presente.
Applicabilità :
Essendo una bibita originale del marchio Coca cola, l’analisi è sempre effettuabile.
Apparecchiatura :
Elettrodo a vetro combinato
Riscaldatore elettrico
Agitatore magnetico
Titolatore automatico
pHmetro tarato
Reagenti :
NaOH 0,1 N
Se non è già pronta la soluzione viene preparata nel seguente modo:
Trasferire il contenuto della fiala di idrossido di sodio, contenente esattamente una mole di base, in un matraccio tarato da un litro, portare a volume con acqua distillata, lavando la fiala affinchè non venga persa della soluzione. Agitare e diluire successivamente portando la soluzione a 0,1 N.
Coca cola
Procedimento :
Travasare il contenuto di una lattina ( pari a 33 cl ) in un becher da 250 ml e porre a riscaldare tramite riscaldatore elettrico. Sotto leggera agitazione, ad una temperatura di circa 35°C, si deve eliminare l’anidride carbonica presente (questa operazione dura circa 10-15 minuti).
Eliminata la CO2, prelevare 50 ml di coca cola e porre in un altro becher. Disporre quindi l’ elettrodo e il titolatore in modo tale da rendere più facile lo svolgimento dell’analisi.
Utilizzando NaOH titolare quindi l’acido fosforico presente in soluzione.
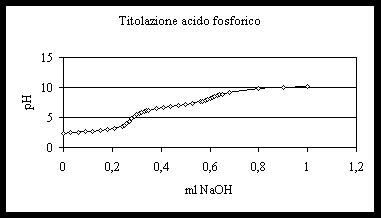
Risultati ottenuti :
| ml NaOH | pH | D pH/D ml | D 2pH/D ml2 |
| 0 | 2.37 | ||
| 0.03 | 2.42 | ||
| 0.06 | 2.5 | ||
| 0.09 | 2.59 | ||
| 0.12 | 2.68 | ||
| 0.15 | 2.79 | ||
| 0.18 | 2.94 | ||
| 0.21 | 3.14 | ||
| 0.24 | 3.5 | ||
| 0.25 | 3.65 | ||
| 0.255 | 28 | ||
| 0.26 | 3.93 | 500 | |
| 0.265 | 33 | ||
| 0.27 | 4.26 | 1700 | |
| 0.275 | 50 | ||
| 0.28 | 4.76 | -300 | |
| 0.285 | 47 | ||
| 0.29 | 5.23 | -1500 | |
| 0.295 | 32 | ||
| 0.3 | 5.55 | ||
| 0.31 | 5.74 | ||
| 0.32 | 5.9 | ||
| 0.33 | 6.01 | ||
| 0.34 | 6.14 | ||
| 0.35 | 6.25 | ||
| 0.38 | 6.45 | ||
| 0.41 | 6.66 | ||
| 0.44 | 6.82 | ||
| 0.47 | 6.99 | ||
| 0.5 | 7.15 | ||
| 0.53 | 7.36 | ||
| 0.56 | 7.62 | ||
| 0.565 | 11 | ||
| 0.57 | 7.73 | 0 | |
| 0.575 | 11 | ||
| 0.58 | 7.84 | 500 | |
| 0.585 | 16 | ||
| 0.59 | 8.01 | 1000 | |
| 0.595 | 13 | ||
| 0.6 | 8.13 | -100 | |
| 0.605 | 23 | ||
| 0.61 | 8.36 | 400 | |
| 0.615 | 13 | ||
| 0.62 | 8.49 | ||
| 0.63 | 8.66 | ||
| 0.64 | 8.81 | ||
| 0.65 | 8.91 | ||
| 0.68 | 9.22 | ||
| 0.8 | 9.83 | ||
| 0.9 | 10.06 | ||
| 1.0 | 10.21 |

Calcoli :
1° PUNTO DI EQUIVALENZA
Derivata seconda=0.27ml+(0.01x1700) / (1700-(-300))=0.2785ml
2° PUNTO DI EQUIVALENZA
Derivata seconda=0.60ml+(0.01x1000)/(1000-(-1000))=0.605ml
N H3PO4 = V NaOH x M NaOH x 3 eq/l / V H3PO4=0.0167 eq/l
Conclusioni :
Dai calcoli sopra riportati si può notare come la concentrazione di acido fosforico presente in soluzione sia davvero molto bassa.
In ogni caso la titolazione è riuscita, e dal grafico si possono notare bene i due salti in corrispondenza dei primi due punti di equivalenza. A causa di una 3° Ka molto bassa (10-13) non è possibile cogliere il terzo salto.
Considerazioni :
E’ facile notare come la tabella sia costituita da molti punti. Questo problema nasce dalla necessità di titolare acido fosforico a bassa concentrazione con una base molto concentrata (non a caso il viraggio avviene aggiungendo solamente 1 ml di titolante). Sarebbe stato più opportuno lavorare con NaOH più diluito.
Un’altra considerazione va fatta: il riscaldamento della bibita per l’eliminazione della CO2 va eseguito a temperature non superiori ai 40°C; al di sopra di quel limite il caramello presente potrebbe dare delle reazioni ed influenzare cosi’ il pH della soluzione.