Determinazione del ferro nella cioccolata
Principi
I processi di lavorazione della cioccolata prevedono diversi trattamenti, fra i quali la macinazione dei grani essiccati o tostati. Durante questi processi i prodotti si arricchiscono di ferro secondo lo stato di usura dei macchinari impiegati.
Il prodotto alimentare viene macinato e incenerito. Si determina poi il ferro sulle ceneri, riprese con HCl dopo avere neutralizzato la soluzione campione.
Applicabilità
Questa è un’analisi abbastanza semplice e può essere applicata a qualsiasi tipo di cioccolata presente sul mercato.
Apparecchiature
crogiolo di porcellana da 20ml
becco bunsen e cappa aspirante
muffola
piastra elettrica riscaldante
matracci tarati da 50 e 100 ml
spettrofotometro doppio raggio
cuvette di vetro
pipette graduate
Reagenti
HNO3 al 65%
HCl 1:2 in acqua distillata
NaOH al 20%
Fenolftaleina allo 0,1% in etanolo
Soluzione standard concentrata di ferro ( 200mg/l )
Pesare 0,200g di filo di ferro purissimo; portare in soluzione con 10ml di H2SO4 1:5 riscaldando debolmente e portando a volume in matraccio tarato da 1L.
Soluzione standard diluita di ferro (10mg/l)
Diluire 50ml della soluzione precedente a 1L in matraccio tarato.
Soluzione di idrossilammina cloridrato (NH2OH*HCl) al 10%
Soluzione di o-fenantrolina allo 0,5%
Soluzione tampone
Sciogliere 250g CH3COONH4 in 150ml di acqua e aggiungere 700ml di CH3COOH glaciale.
Procedimento
Pesare accuratamente in un crogiolo 1,44 g di cioccolata.
Carbonizzare il campione prelevato in muffola a 550°C. Dopo circa 3 ore (quando le ceneri sono diventate quasi bianche) togliere il crogiolo dalla muffola e lasciare raffreddare: versare poi 1-2ml di HNO3. Porre il crogiolo su piastra elettrica riscaldante fino a completa evaporazione di HNO3 e trasferire di nuovo in muffola a 550°C.
Riprender le ceneri bianche e raffreddate con 10ml di HCl e lasciare di nuovo su piastra elettrica riscaldante per circa mezz’ora.
Raffreddare e trasferire la soluzione con acqua distillata in un matraccio tarato da 100 ml e portare a volume.
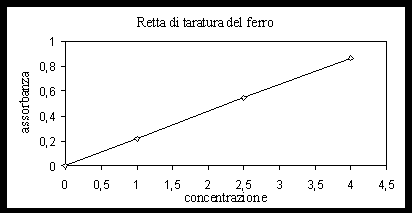
Retta di taratura del ferro e bianco reagenti:
Trasferire in 6 matracci tarati da 100 ml, 1-5-15-25-35-45 ml della soluzione diluita di ferro. Aggiungere un po’ di acqua distillata, 2 ml di HCl concentrato e 1 ml di idrossilammina . Attendere 10 min in modo che la riduzione di Fe (III) a Fe (II) sia completa. Aggiungere 10 ml di tampone e 2 ml di o-fenantrolina e portare a volume con acqua distillata. Preparare il bianco reagenti secondo le stesse modalità, ma escludendo la soluzione di Fe (II). Dopo circa 20 minuti dall’aggiunta dell’o-fenantrolina leggere l’assorbanza a 510 nm contro acqua distillata. Si ottiene così la retta di taratura del ferro.
Infine leggere l’assorbanza della soluzione contenente la cioccolata con lo spettrofotometro.

equazione della retta Y = ( 1,191901 x 10-4 ) + ( 2.149900 x 10-1 ) x X
Risultati ottenuti
A 510 nm è risultata un’assorbanza pari a 0,0744.
Calcoli
Sostituendo questo valore nell’equazione della retta ricaviamo la concentrazione ( C ) in mg/l di Fe presente nel campione:
Fe cioccolata = 0,0665 mg/l
OOOOOOOOOOOC x 10000
Fe (mg/Kg) = _______________
OOOOOOOOOOOVx x m
C = concentrazione di Fe in mg/l ricavata dalla retta di taratura
m = massa del campione in g
Vx = volume in ml di soluzione cloridrica prelevata per l’analisi
Fe (mg/Kg) nella cioccolata = 46,18mg/Kg
Osservazioni
Dai risultati ottenuti si può notare che la concentrazione di ferro nella cioccolata ha valore più che doppio di quella relativa al caffè ( vedi analisi del ferro nel caffè presentata nella relativa sezione ). Se durante la lavorazione, questi prodotti si arricchiscono di ferro a seconda dello stato di usura dei macchinari utilizzati si può dedurre che lo stato di usura di quelli utilizzati per lavorare la cioccolata da noi analizzata era decisamente più elevato di quello dei macchinari usati per la lavorazione del caffè.